Për herë të parë ky term është përdorur nga filozofi i Greqisë së lashtë Demokriti (460 p.e.s.-370 p.e.s.) i cili me këtë fjalë emërtonte atë element të materies që nuk ndahet më d.m.th atomi greqisht atomo (±Ä¿¼¿) = fjalë e përbërë nga parafjala a=pa + tomo, temno=presë, ndaj, ajo që nuk pritet më.
Atomi është grimca më e vogël që ndërton cdo substancë. Një substancë e thjeshtë përbëhet nga atome të të njëjtit lloj. Më pas Xhon Daltoni i vërtetoi botëkuptimet e filozofëve Demokriti dhe Leukipi. Ai doli në përfundim se materia është e ndërtuar prej grimcave të vogla të cilat nuk mund te ndahen prej tij me metoda kimike.
Këto grimca janë atomet. Kemi edhe eksperimentin e Radhërfordit. Ai mori një fletë ari dhe e bombardoi atë me rreze alfa. Kur rrezet shkuan në qendër, ato devijuan. Shkaku ishte se kishte protone me ngarkesë pozitive dhe afër ishin protonet të cilat janë pa ngarkesë. Rreth bërthamës rrotullohen elektronet të cilat janë pa ngarkesë.
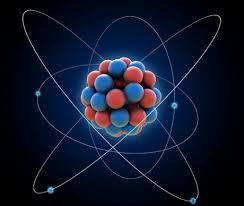
Atomi është i përbërë nga bërthama dhe elektronet me ngarkesë elektrike negative që rrotullohen rreth saj, në brendësinë e bërthamës gjejmë neutronet që janë thërrmija pa ngarkesë elektrike dhe protonet me ngarkesë elektrike pozitive. Për çdo atom në gjendje normale numri i protoneve është i barabartë me numrin e elektroneve. Kur numri protoneve është i barabartë me numrin e elektroneve atëherë themi që atomi është neutral.
Ndërsa kur atomi humb një ose më shumë elektrone ngarkesa e tij nuk është më neutrale (zero), sepse duke humbur ngarkesat negative të elektroneve, atij i kanë mbetur vetëm ngarkesat pozitive të protoneve në bërthamë, atëherë themi se atomi është shndërruar në një jon pozitiv ose kation.
Ndërsa, kur atomit i bashkohen një ose më shumë elektrone, ky nuk është me neutral, sepse i janë shtuar elektrone me ngarkesa negative, pra edhe një herë kemi të bëjmë me shndërrimin e një atomi në një jon por kësaj radhe jon negativ ose anion.
Që atomi është i pandashëm mund të thuhej kur ne nuk e njihnim akoma natyrën e një atomi, tani mund te konfirmojmë që atomet janë të ndashëm sepse edhe humbja e një elektroni do te thotë ndarje e tij. Për më tepër shkenca ka ecur shumë përpara saqë tani është e mundur edhe ndarja e bërthamës së një atomi, ky veprim quhet fision nuklear dhe është i mundur në centralet nukleare.
Atomet e elementve të ndryshëm bashkëveprojnë ndërmjet tyre dhe gjatë këtij bashkëveprimi njëri nga elementët ka aftësi të japë elektrone, ndërsa elementi tjetër është i prirur të marrë elektrone në shtresën e jashtme. Atomet janë grimca të imëta të materies.
Secili lloj i atomeve ka masën e caktuar. Për shembull masa e atomit të hidrogjenit është e njohur.
Ajo është e përbërë nga: protonet (p-), elektronet (e+), neutrone(n0).
Meqënëse atomet jane grimca shumë të imta, masat e tyre nuk mund të maten me peshore. Peshoret më të sakta janë peshoret e kuarcit që kanë njësi të rendit nano 10 në fuqi -9. Për këtë arsye duhet të përdoret një njësi e përshtatshme për matjen e tyre. Masa e elektronit është 9,1*10 në fuqi -28g. Masa e protonit është 1,673*10 në fuqi -24g. Ndërsa masa e neutronit është afërsisht sa masa e protonit 1,675*10 në fuqi -24g.